|
2006年11月1日発行 第135巻・臨時増刊号 目次 |
■PDF(135巻・臨時増刊号)
臨床試験のABC
135巻・臨時増刊号のPDFの入り口はこちらのみとなります。
…… [ PDF 5.04M] PDF 5.04M]
注)以下の目次の各項目からはリンクがありません。
■序
唐澤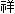 人 人
……6
■1 臨床試験と治験
1 治験と医薬品の開発
西岡 清
……16〜21
2 臨床研究と臨床試験と治験
下山正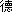
……22〜28
3 わが国における治験の現状と問題点
景山 茂
……29〜33
4 医師主導治験と臨床試験
福田治彦
……34〜39
5 日本医師会治験促進センターの果たす役割
寺岡 暉
……40〜45
■2 臨床試験と倫理
1 生命倫理の過去・現在・未来─研究倫理を中心に
前田正一・赤林 朗
……48〜53
2 ヘルシンキ宣言と各種臨床試験倫理指針について
渡邉裕司
……54〜58
3 臨床試験と個人情報保護法
樋口範雄
……59〜63
■3 医薬品と特殊領域における開発フェーズ
1 第I相試験
中野重行
……66〜70
2 第II相試験
砂川慶介・佐藤淳子
……71〜76
3 第III相試験
楠岡英雄・森下典子
……77〜81
4 第IV相試験
山本晴子
……82〜86
5 小児の治験
伊藤 進・河田 興
……87〜92
6 悪性腫瘍の治験
土井美帆子・藤原康弘
……93〜97
7 医療機器の治験
佐瀬一洋
……98〜103
■4 医療統計学と臨床試験成績の読み方
1 医療統計学の基本
浦島充佳
……106〜110
2 臨床試験成績の読み方
名郷直樹
……111〜114
■5 治験薬
1 プラセボとは
川合眞一
……116〜117
2 治験薬と毒薬・劇薬
日 慎二 慎二
……118〜119
3 生物製剤
鹿野真弓
……120〜121
4 ファーマコゲノミクス(薬理遺伝学)
辻本豪三
……122〜124
■6 医薬品・医療機器の製造販売承認
1 治験と医薬品・医療機器の製造販売承認制度
平山佳伸
……126〜130
2 医薬品医療機器総合機構の役割
上田慶二・山田博史
……131〜136
■7 海外の臨床試験
1 海外における医薬品開発
小林利彦
……138〜140
2 日米EU医薬品規制調和国際会議と外国臨床データ
森 和彦
……141〜143
3 海外の臨床試験
鎌倉孝行
……144〜146
■8 臨床試験に参加するには
1 臨床試験に参加することの意義
矢崎義雄
……148〜153
2 臨床試験を始めるときの心得
島田安博
……154〜158
3 医薬品の臨床試験の実施の基準(GCP)
小野俊介
……159〜164
■9 臨床試験プロトコル
1 プロトコルの読み方
岸本淳司・山崎 力
……166〜169
2 臨床試験審査委員会(IRB)の役割
小林真一
……170〜174
3 同意説明文書
伊藤澄信
……175〜179
4 治験薬概要書の読み方
大橋京一・小手川勤
……180〜184
5 医師主導治験と企業治験
中村秀文
……185〜190
6 有効性評価と安全性評価のガイダンス
宇山佳明
……191〜201
7 補償と賠償
辻純一郎
……202〜204
■10 臨床試験を支援する職種と業務
1 治験コーディネーター
和泉啓司郎・江口久恵
……206〜212
2 モニタリングと監査
横田雅彦
……213〜217
3 CROとSMO
成川 衛
……218〜220
■11 臨床試験に関連する法的諸問題
1 薬事法
山田雅信
……222〜225
2 麻薬及び向精神薬取締法
村上貴久・富永俊義
……226〜228
3 医薬品副作用被害救済制度
宮崎生子
……229〜233
■巻末資料
薬事法(抄)
……250〜254
薬事法施行規則(抄)
……254〜257
医薬品の臨床試験の実施の基準(GCP)
……258〜275
同意説明文書の雛形
……276〜286
医薬品等の副作用の重篤度分類基準について
……287〜296
有害事象共通用語規準(CTCAE)v3.0
……297〜344
|